§ 25. Электралітычная дысацыяцыя рэчываў у растворах
Дысацыяцыя злучэнняў з кавалентным палярным тыпам сувязі
Большасць арганічных і неарганічных кіслот растваральныя ў вадзе і з’яўляюцца электралітамі. У кіслотах атамы вадароду звязаны кавалентнымі палярнымі сувязямі з атамамі кіслотных астаткаў. У палярных малекулах гатовых іонаў няма. Разгледзім працэс дысацыяцыі кіслот на прыкладзе малекулы .
Спачатку палярныя малекулы кіслаты прыцягваюцца да палярных малекул вады і яшчэ больш палярызуюцца.
Утвараюцца вадародныя сувязі паміж малекуламі кіслаты і вады (мал. 58).
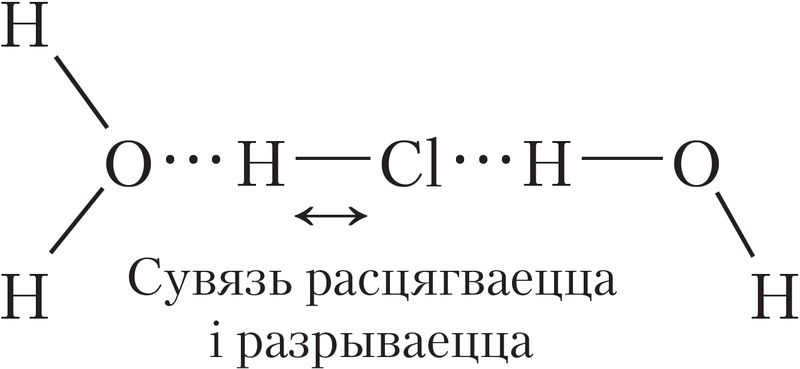
Затым кавалентная палярная сувязь падаўжаецца і становіцца менш трывалай. У выніку яна разрываецца, гэта значыць адбываецца ўтварэнне іонаў:
Атрыманы пры дысацыяцыі кіслаты катыён H+ далучаецца да малекулы вады з утварэннем катыёна гідраксонію H3O+ па донарна-акцэптарным механізме, з якім вы пазнаёміліся, вывучаючы матэрыял § 13.
Іон хлору, што ўтварыўся пры іанізацыі, таксама аказваецца гідраціраваным, што паказана на малюнку 57.
Для спрашчэння ўраўненняў рэакцый у іоннай форме звычайна запісваюць гідраціраваны катыён вадароду ў выглядзе Н+.
Аналагічным чынам пад дзеяннем палярных малекул вады адбываецца дысацыяцыя і іншых злучэнняў з кавалентным палярным тыпам сувязі.
Дысацыяцыя ўключае працэсы гідратацыі зыходных малекул, іх палярызацыі, разбурэння сувязей у малекулах і іх распаду з утварэннем гідраціраваных іонаў.
Малекулы кіслот пры дысацыяцыі ў водных растворах поўнасцю або часткова дысацыіруюць на катыёны вадароду і аніёны кіслотных астаткаў: