§ 9. Стан электрона ў атаме
Пытанні, заданні, задачы
1. Назавіце характарыстыкі электрона:
- а) як часціцы;
- б) як хвалі.
2. Назавіце спосабы адлюстравання размеркавання электронаў у атаме азоту:
- а) 7N 2е–,5е–;
- б) 7N 1s22s22p3;
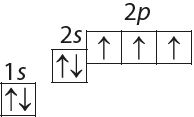
- в) 7N
3. Як зменіцца энергія электрона, калі яго перавесці са стану з n = 2 у стан з n = 3? Што адбудзецца з энергіяй электрона, калі ён вернецца ў ранейшы стан?
4. Выкарыстоўваючы малюнак 18, расстаўце наступныя атамныя арбіталі ў парадку павелічэння іх энергіі: 3p, 2p, 3d, 1s.
5. У якім стане энергія электрона вышэйшая: 2s або 2p; 3p або 2p?
6. Чым адрозніваюцца атамныя арбіталі 1s і 3s?
7. Колькі ўсяго электронаў можа знаходзіцца на трэцім энергетычным узроўні, на 1s-падузроўні, на 2р-падузроўні, на 3d-падузроўні?
8. Пры ўзбуджэнні электрон перайшоў з 2s- на 2р-арбіталь. Што пры гэтым змянілася:
энергія электрона, форма электроннага воблака, зарад атама, энергія атама?
9. Разлічыце лік электронаў у порцыі фосфару масай 1,24 г.
10. Порцыя нітрату двухвалентнага металу колькасцю 0,2 моль змяшчае 16,4 моль электронаў. Вызначце элемент.